La aragonita se transforma en calcita a temperaturas entre los 380 y 470 ° C, mientras que la vaterita es aún menos estable.
Se puede reconocer fácilmente por la efervescencia que siempre produce con ciertos ácidos, como el ácido clorhídrico o el vinagre, así como por su dureza.
Presenta diversas coloraciones muy variadas que reflejan
El mineral tiene una amplia distribución a escala global y es empleado para diferentes usos, desde lentes hasta materiales de construcción.
Plinio la llamó así ya en el año 79, del latín calx, «cal viva». A veces se utiliza como sinónimo «piedra caliza», si bien la caliza es en realidad la roca formada mayoritariamente por este mineral.
Etimología
Fórmula quimica: CaCO3
Dureza: 3 en la escala de Mohs
Color:Se puede encontrar en color blanco u otras variedades, dependiendo de las impurezas.
Clase Minera: V. Oxisales, dentro de los carbonatos.
Densidad: De 2,710 a 2,711 g/cm3
Sistema Cristalino: Romboedrico
El nombre fue introducido en 1849 por el mineralogista austríaco Wilhelm Karl von Haidinger; lo hizo combinando la palabra alemana calzado y el sufijo -ita (en alemán -it) que es habitualmente empleado para llamar minerales.
La palabra calcio derivaba del latín calx (que en catalán significa «cal»). Plinio el Viejo ya llamó calx la calcita en 79 dC.
El término «alabastro» es también utilizado por arqueólogos y profesionales del comercio de piedra para referirse a una variedad de calcita de grano fino que aparece en depósitos agitados. Este término no mantiene relación con el término «alabastro» para referirse a la variedad de yeso.
Clasificación de la calcita
Según la clasificación de Nickel-Strunz, la calcita mineral pertenece a «05.AB: carbonatos sin aniones adicionales, sin H2O, alcalinotérreos (y otros M2 +)» junto con los siguientes minerales: gaspeïta, magnesita, otavita, rodocrosita, siderita, smithsonita, esferocobaltita, ankerita, dolomita, kutnohorita, minrecordita, aragonita, cerussita, estroncianita, witherita, vaterita, huntita, norsethita, alstonita, olekminskita, paralstonita, baritocalcita, carbocernaïta, benstonita y juangodoyita. Según la clasificación de Dana la calcita es un carbonato clasificado en el grupo 14.1.1.1: carbonatos anhidros normales de fórmula A (XO3).
Identificación
Debido a la efervescencia que siempre produce con los ácidos, se ha comprobado que una de las maneras más efectivas para identificar
Un ejemplo del uso de este test es la verificación de si un cemento de gres o de conglomerado es de calcita o no, ya que en caso de que haga efervescencia se podrá afirmar que el cemento contiene este mineral calcita.
El motivo de este hecho es la siguiente reacción química, en la que el dióxido de carbono produce burbujas en escaparse en forma de gas: CaCO3 + 2H + → Ca + 2 + H2O + CO2 (g).
Para realizar el test, es importante que el ácido clorhídrico se encuentre concentrado al 10%; esto es debido a que en concentraciones superiores, el ácido también puede hacer hervir algunas dolomías (formadas por dolomita), y por tanto conllevar confusión. Además del test del ácido, la calcita se puede identificar por su dureza, pudiéndose rayar con una moneda de cobre.
Debido a su dureza (dureza = 3), fue escogido como mineral de referencia en la escala de Mohs. Los minerales calcita suelen presentar maclas, tan simples como múltiples, un brillo vítrea y una raya de color blanco. Puede presentar varios colores, algunos de los cuales son blanco, amarillo, marrón, rojo, azulado o negro.
Su hábito puede ser característico sobre todo cuando la calcita se encuentra bien cristalizada.
Maclado

Con microscopio óptico
La calcita observada con microscopio óptico es uniaxial con un signo óptico negativo; su orientación óptica (X | c) es difícil de determinar 
Puede presentar maclado simple y lamelar en algunas caras cristalinas. Presenta exfoliación romboédrica muy clara y perfecta, siempre visible, excepto en los agregados micrítics. La extinción de la calcita es recta en agregados columnares y simétrica en el Romboedro de exfoliación. En el microscopio también es posible observar las macles polisintéticas laminares (no siempre presentes) paralelas a la diagonal mayor del Romboedro de exfoliación.
Propiedades de la calcita
Color
La piedra calcita pura, extremadamente raro en la naturaleza, es incolora y transparente. A menudo, la calcita presenta impurezas (otros elementos que entran dentro de su estructura cristalina); estas impurezas pueden hacer variar el reo rango cromático.
Dejando de lado el espato de Islandia, una de las curiosidades de la calcita es que suele presentar coloraciones amarillentas o marrones cuando se encuentra en estado natural. Algunos de los elementos que pueden hacer variar su color son el hierro, el zinc, el cobalto o el manganeso.
Cuando la calcita tiene hierro, ésta presenta coloraciones amarillentas o marrones (se puede comparar con la siderita (FeCO3)); el zinc produce coloraciones grisáceas en la calcita (se puede comparar con el smithsonita (ZnCO3)); el cobalto produce coloraciones rosadas (se puede comparar con el esferocobaltita (CoCO3)); finalmente, el manganeso, produce colores violetas o rosadas (se pueden comparar con la rodocrosita (MnCO3)).
Las calcitas también pueden presentar coloración verde, a menudo localizada en una parte de los cristales; esto se debe a menudo a la presencia de malaquita de color verde oscuro, que, mezclada con calcita, genera el color verde. Un ejemplo de calcita verde por la acción de la malaquita se encuentra al este del estado de Querétaro, en el centro de México.
Los colores del rango entre el azul cielo y el color de lavanda son a menudo producidos por la radiación producida por algunos minerales. Esta radiación produce defectos en la red cristalina; estos defectos provocan diferentes absorciones de la luz que consecuentemente generan el color azul.
Estructura cristalina de la Calcita
La estructura de la calcita no es muy compleja y, por tanto, se puede entender fácilmente observando un esquema o dibujo.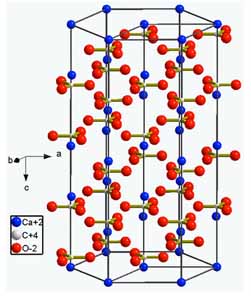
Mientras que en la halita alternan los iones de sodio y de cloro, en la calcita se alternan los de calcio y los carbonatos (CO2-3).
A diferencia de la halita, la calcita no es un mineral cúbico como consecuencia de los iones carbonato, que rompen la simetría cúbica en varios sentidos; uno de los cuales es la orientación de las diferentes moléculas de carbonato, que rompen la simetría cúbica y transforman el cubo en un Romboedro (un cubo con uno de los ejes variados).
La calcita presenta una estructura similar a todos los integrantes del grupo de la calcita de minerales; estos integrantes están formados por carbonato y metales divalentes de radio inferior a 1; en este caso, los átomos de carbono se encuentran de manera trigonal planar en el CO2-3, mientras que los metales divalentes se encuentran en coordinación octaédrica. El grupo puntual de la calcita es 3m, mientras que el grupo espacial es R-3c.
La estructura de la calcita puede presentar diversas variaciones a elevadas presiones: a 1,5 GPa se convierte en calcita-II, una variedad monoclínica P21 / c con una celda a = 6,334; b = = 4,948; c = 8,033 y β = 107,9º. A 22 kbar, la calcita-II se convierte en calcita-III, otra variedad monoclínica C2 con una celda a = 8,746; b = 4,685; c = 8,275; β = 94,4; y Z = 6. La calcita-II y la calcita-III son relativamente metaestables con la aragonita, la cual es estable hasta 8 GPa.
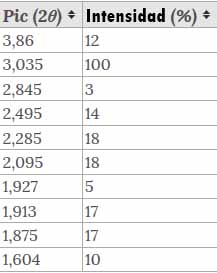
La calcita es un polimorfo del aragonita y la vaterita, siendo el polimorfo más estable del carbonato de calcio. Tanto el aragonito como la vaterita tienen la misma fórmula química pero una estructura cristalina diferente, y son más solubles: la aragonita se transforma en calcita a 400 ° C, y la vaterita (mineral muy raro), o μ-CaCO3 , es aún menos estable. Es isostructural con la nitratina y el otavita, y forma una serie de solución sólida con la rodocrosita. Cuando se somete un cristal o masa de calcita en difracción de rayos X, se obtienen diferentes picos de intensidades de energía:
Propiedades físicas de la Calcita
La calcita es un mineral de carbonato cálcico que cristaliza en el sistema trigonal, presentando formas cristalinas muy variables (sobre todo el Romboedro, forma en la que se exfolia fácilmente, y el escalenoedre).
Sus macles son muy frecuentes según {1000} y {101}, tiene tanto de simples como de polisintéticas, además de agregados en drusas y geodas.
La dureza de la calcita es de 3 en la escala de Mohs, y una densidad de 2,710 a 2,711 g / cm3. Su brillo es más bien vítrea, aunque a veces también satinada.
Este mineral menudo presenta un aspecto transparente y opaco, aunque también puede ser incoloro, blanco, amarillo, rosa, rojo, naranja. Su raya es blanca.
Propiedades químicas
Su fórmula química es CaCO3. Los elementos que se encuentran en su estructura son el calcio, el carbono y el oxígeno.
Algunos elementos pueden entrar en su estructura como impurezas; algunos de estos elementos son manganeso, hierro, zinc, cobalto, bario, estroncio, plomo, magnesio, cobre, aluminio, níquel, vanadio, cromo y molibdeno.
En el caso del cobalto, el Co2 + le da una coloración rosa. La calcita, como la mayoría de carbonatos, se disuelve en la mayoría de ácidos.
También puede ser disuelta por diferentes tipos de agua, dependiendo de diferentes factores tales como la temperatura del agua, el pH, y la saturación de la misma.
Aunque la calcita es casi insoluble en agua fría, un bajo pH del agua puede provocar la disolución de la calcita.
La calcita presenta un raro disparo, llamado solubilidad retrógrada, en el que se convierte en menos soluble en agua conforme la temperatura de esta aumenta.
Cuando las condiciones son buenas para la precipitación de calcita, esta forma cementos que rellenan fracturas o porosidades.
Cuando las condiciones son buenas para la disolución, la calcita de las fracturas y la porosidad se elimina, y si las condiciones favorables a la disolución perduran en el tiempo, incluso se pueden formar grandes porosidades como cuevas (karsts).
La calcita también tiene una elevada reactividad incluso con ácidos débiles como el vinagre, ya que hace efervescencia con los ácidos diluidos fríos.
Propiedades ópticas
La calcita es un mineral transparente o translúcido que, como ya se ha mencionado anteriormente, puede presentar una gran gama de colores: incoloro, blanco, amarillo, marrón, rojo, azulado a negro.
En lámina delgada presenta colores de interferencia elevados en polarización cruzada. La clase óptica es uniaxial (-).

Los cristales individuales de calcita presentan la propiedad óptica llamada birrefringencia (refracción doble).
La fuerte birrefringencia de algunos cristales provoca que los objetos que se miren a través de un trozo de calcita se vean dobles.
Este efecto fue descrito por primera vez por el científico danés Rasmus Bartholin en el año 1669.
Además de birrefringencia, la calcita puede presentar fluorescencia; en onda larga (365 nm) a menudo presenta colores rosas, aunque puede llegar a presentar los colores blanco, blanco azulado, blanco amarillento, blanco rosado, amarillo, amarillo anaranjado, naranja, rojo, violeta, rosa salmón, amarillo verdoso, azul , blanco verdoso y azul violáceo.
En onda media (320 nm), la calcita suele presentar fluorescencia roja, aunque puede presentar de blanca, blanco azulado, blanco amarillento, rojo anaranjado, verde amarillento y azul verdoso. En onda corta (254 nm) la calcita presenta fluorescencia azul; además puede presentar los colores blanco, blanco azulado, blanco amarillento, blanco rosado, amarillo claro, amarillo anaranjado, naranja, rojo, rosa, rosa salmón, verde, verdoso, azulado, blanco verdoso y amarillento.
En todos los casos la intensidad de la fluorescencia es fuerte.
La calcita, a veces, también presenta fosforescencia, es decir, que tiene la capacidad de absorber y almacenar energía para luego liberarla en forma de luz.
A veces también presenta termoluminiscencia, producida por la liberación de luz después de ser sometida a temperaturas elevadas. En este caso, la temperatura debe oscilar entre los 50 y 200 ºC (temperatura bastante inferior a la temperatura de incandescencia).
Celda unidad
En cualquier cristal (no sólo los cristales de calcita) las moléculas y los átomos se distribuyen en redes regulares.
La morfología del cristal se basa principalmente en este enrejado que está formado por una repetición periódica de los motivos.
Generalmente es muy complicado encontrar la relación entre la geometría de los motivos y la del cristal. Es por ello que en cristalografía se suele emplear otro método: a partir de la celda unidad.
La celda unidad es la fracción espacial más pequeña de un cristal que presenta todas las propiedades de simetría de este.
En el caso de la calcita, las dimensiones de la celda unidad son de 4,9896 Å para el eje ay 17.061 Å para el eje c (con un ratio en: C = 1: 3.419).
Cuando se dan los valores de las dimensiones de la celda unidad, también es habitual dar el valor de Z; Z es el número de unidades de fórmula que se encuentran en la celda unidad.
En el caso de la calcita, la Z = 6; es decir, que dentro de la celda hay seis unidades de fórmula.
Antes del uso de los rayos X en cristalografía, los ejes cristalinos se determinaban midiendo los ángulos entre caras, escogiendo los ángulos más pequeños, asumiendo que las caras más grandes presentaban ordenamiento más básico.
Con este método, habitualmente coincidían los valores con los descubiertos posteriormente mediante los rayos X.
Esto no pasó en el caso de la calcita. Originalmente la calcita se le asignaba un ratio de celda c: a = 0,8543, siendo c hasta cuatro veces superior al valor obtenido con rayos X; actualmente se considera que c: a = 3,419.
En la mayoría de índices de Miller de la calcita, obtenidos antes de la aplicación de los rayos X, el valor c se multiplicará por cuatro.
Por ejemplo, la exfoliación romboédrica es perfecta en {1011} (en la versión antigua) y es perfecta en {1014} en la versión actual (la versión correcta y aceptada)
Formacion
La calcita es un mineral que se forma por precipitación química mediante la evaporación de soluciones muy ricas en hidrogenocarbonato de calcio o por la extracción y la actividad de los organismos marinos y de agua dulce.
La calcita es un mineral muy común, ya que tiene una amplia distribución por todo el planeta, y se calcula que ocupa aproximadamente el 4% del peso total de la corteza terrestre y que recubre el 40% de su superficie.
Se encuentran canteras por todo el mundo, a los suelos, a las costras desérticas, a las fuentes hidrotermales, los yacimientos metasomàtics, a las pegmatitas, en las zonas de meteorización y de oxidación, los espeleotemas e incluso en ciertas rocas magmáticas.
Es un componente habitual de las rocas sedimentarias, especialmente la caliza, aunque es muy fácil de encontrarla asociada a diversos minerales como la siderita, el cuarzo, la pirita o la fluorita.
Como mineral que se forma por precipitación, para entender el proceso de información, se debe comprender primero el comportamiento del carbonato cálcico en las diferentes condiciones.
Generalmente, este comportamiento (por ejemplo en el caso de la calcita) viene determinado por la ecuación:
Donde CaCO3 es calcita en estado sólido; H2CO3 es ácido carbónico (formado por la reacción entre el agua y el dióxido de carbono [H2O + CO2 = H2CO3]); Ca + 2 es el ión positivo calcio (catión) en solución, y HCO-3 es el ión negativo (anión) hidrogenocarbonato (llamado antiguamente ión bicarbonato) en solución.
Como consecuencia de que el equilibrio es dinámico, las ecuaciones CaCO3 + H2CO3 = Ca + 2 + 2HCO-3 y H2O + CO2 = H2CO3 se encuentran estrechamente relacionadas.
Si se aumenta el CO2 en la segunda ecuación, se producirá más H2CO3 (en ningún caso tomamos el agua como reactivo limitante, ya que en un lago o en el océano se encuentra en enormes cantidades).
Este incremento de H2CO3 implicará una disolución de la calcita (CaCO3). Por lo tanto, al igual que si aumentamos el contenido de CO2 en un agua la calcita se disuelve, si disminuimos el contenido, la calcita precipitará.
Es por este motivo que la calcita precipita en los casos donde un agua cargada con CO2 disuelto lo libera a la atmósfera.
Esta ecuación también nos ayuda a comprender las condiciones ambientales de precipitación de la calcita.
Si observamos un mapa de temperaturas marinas y lo comparamos con las zonas actuales de precipitación de calcita, observaremos que las zonas de precipitación coinciden con las de elevada temperatura, y se sitúan cerca de los trópicos.
Esta evidencia se explica porque el CO2, como la gran mayoría de los gases, es menos soluble a temperaturas altas y más soluble a temperaturas bajas.
Este hecho implica que a temperaturas bajas el CO2 disuelto en agua tienda a permanecer disuelto y por lo tanto el carbonato de calcio no precipite.
En cambio, a elevadas temperaturas, el dióxido de carbono pierde solubilidad y es liberado a la atmósfera; en este caso, como consecuencia de la pérdida de CO2, se da la precipitación de la calcita.
Por esta misma razón, hay precipitación de calcita en manantiales calientes o termales, independientemente de su latitud.
Los aumentos en la presión de carga aumentan la solubilidad de los gases, y por tanto también del dióxido de carbono; por tanto, un aumento de la presión producirá una disolución del carbonato de calcio.
Las algas y plantas acuáticas o marinas también tienen un papel importante en la precipitación o disolución del carbonato de calcio, ya que al realizar la fotosíntesis eliminan parte del CO2 de las aguas, y por tanto favorecen la precipitación de la calcita.
Cuando estas mismas plantas mueren y se descomponen, liberan CO2 y, por tanto, favorecen la disolución del carbonato cálcico.
De manera general, los carbonatos minerales precipitan en contextos básicos y se disuelven en condiciones ácidas.
A temperatura y presión atmosféricas (25 ° C y 1 atm), la calcita es termodinámicamente estable. En este contexto, todas las formas metaestables de carbonato de calcio tienden a la transformación en calcita.
La calcita también puede precipitar por la actividad de los organismos marinos que forman sus conchas de carbonato cálcico y que al morir se sedimentan dando lugar a las llamadas calizas organogèniques o bioquímicas.
También se puede encontrar formando parte de rocas formadas por metamorfismo regional o de contacto de calizas sedimentarias que se transforman en mármol por recristalización de la calcita (para más información sobre las rocas constituidas por calcita, véase el siguiente apartado).
La calcita como mineral formador de rocas
Rocas sedimentarias
La calcita es el principal mineral no silicato formador de rocas. Es un importante formador de rocas sobre todo en ambientes sedimentarios, aunque puntualmente tiene cierta influencia en algunos ambientes ígneos y metamórficos, y también lo puede ser en ambientes hidrotermales.
Las principales rocas constituidas mayoritariamente por calcita son algunas rocas carbonatadas, concretamente las calizas. Las rocas calizas suelen tener más de un 50% de calcita, y también pueden contener otros minerales dependiendo de su contexto de formación (arcilla, hematites, siderita, cuarzo).
Si una roca caliza contiene una cantidad relevante de arcilla, esta llama marga. El término entre la caliza y la marga suele llamarse margocalizas.
Las calizas están constituidas por granos minerales de calcita. Algunos de estos fragmentos provienen de fragmentos esqueléticos marinos tales como el coral, los gasterópodos, bivalvos, equinodermos, crinoideos, foraminíferos, algas y otros organismos.
También se encuentran otros fragmentos como ooides, peloides, intraclasts y extraclasts. Hay rocas calizas que no presentan grandes, sino que se encuentran formadas a partir de una precipitación química de calcita; por ejemplo el travertino.
Las rocas calizas se forman en mares y océanos cálidos (en regiones tropicales), sobre todo en zonas donde hay un aporte sedimentario (detrítico) poco importante. Las rocas calizas se pueden diferenciar según su origen; este puede ser químico o biológico.
Origen químico: en el caso de un origen químico, la caliza se forma a partir de la precipitación del carbonato de calcio disuelto en agua con cierto contenido de ácido carbónico (CO2), como consecuencia de la alta solubilidad que presenta el carbonato cálcico.
Cuando las aguas cargadas de CO2, liberan el gas a la atmósfera, se produce una precipitación química del carbonato de calcio en exceso:
Esta liberación del dióxido de carbono se produce en dos contextos diferentes. El primero se da en el litoral, cuando las aguas cargadas en dióxido de carbono llegan a la superficie y este se libera a la atmósfera. El segundo se da cuando las aguas continentales subterráneas llegan a la superficie.
Origen biológico: en el caso del origen biológico, son los organismos marinos los que emplean el carbonato de calcio para construir sus esqueletos minerales.
Para ciertas especies marinas, es fácil adquirir carbonato de calcio, ya que se encuentra de manera abundante en el mar y en algunos lagos, y en ocasiones incluso casi en estado de saturación.
Ciertos organismos inducen la precipitación de la calcita para formar los esqueletos. Cuando estos organismos mueren, los restos minerales se acumulan en el fondo marino.
En algunos casos forman auténticos sedimentos que tras la diagénesis constituirán la mayoría de calizas existentes actualmente en la Tierra.
Rocas ígneas
La calcita puede ser un mineral primario (ígneo) o secundario (formado posteriormente a los procesos ígneos) en rocas ígneas.
En el primer caso, se encuentra en rocas formadas a partir de magmas relativamente ricos en dióxido de carbono, y suele ser un mineral tardío que cristaliza en la matriz de la roca.
En el segundo caso, la calcita se forma por alteración o cristalización a partir de fluidos hidrotermales o meteóricos.
Las rocas ígneas que contienen más de un 50% de carbonato denominan carbonatitas. La calcita también puede estar presente, aunque en menor medida en kimberlitas.
Rocas metamórficas
Cuando cualquiera de las rocas citadas anteriormente es afectada por metamorfismo, se transforma en una roca metamórfica.
Si la roca original presenta cantidades relevantes de calcita o carbonato, es habitual que la roca metamórfica que derive también en presente. La roca metamórfica más conocida que presenta calcita es el mármol.
El mármol se forma a partir de un metamorfismo que causa una recristalización de los carbonatos preexistentes.
El mármol resultante presenta una especie de mosaico tipo Blocky de cristales de carbonato. Las estructuras sedimentarias de la roca original son frecuentemente destruidas, aunque en algunos casos se conservan, e incluso se han encontrado fósiles en mármoles. Cuanto más pura sea la roca caliza original, más puro será el mármol resultante.
La calcita también se encuentra en otras rocas metamórficas como esquistos o filitas carbonatadas o skarns.
La calcita en la historia geológica: los mares de calcita
Los mares de calcita aparecen en la historia de la Tierra cuando los precipitados inorgánicos marinos de carbonato de calcio eran bajos en magnesio (LMC; del inglés Low Magnesium Calcite), opuesto a los actuales ricos en magnesio del aragonita (HMC; de del inglés High Magnesium Calcite).
Los mares de calcita alternaban con los de aragonita siendo más prominentes en los períodos Ordovícico y Jurásico. La mineralización obtenida en aquellas épocas aún aprecia.
Un mar de calcita es aquel donde el principal carbonato de calcio inorgánico que precipita es la calcita con bajo contenido de magnesio; en contraposición, un mar de aragonita es todo aquel mar donde el principal carbonato de calcio inorgánico que precipita es la aragonita con elevado contenido de magnesio.
Como ya se ha especificado anteriormente, durante el Paleozoico inferior y desde el Mesozoico medio al Mesozoico superior, predominaban claramente los mares de calcita, destacando sobre todo los mares de calcita del Ordovícico y el Jurásico. Los mares de aragonita eran frecuentes en el Paleozoico medio, al Mesozoico inferior y al Cenozoico (también en la actualidad).
Los principales efectos geológicos y biológicos de las condiciones de los mares de calcita incluyen la rápida y amplia formación de tierras duras carbonatadas, ooides calcítics, cementos de calcita, y la disolución contemporánea de las conchas aragonítiques en mares cálidos.
Las tierras duras son muy comunes, por ejemplo, en los mares de calcita del Ordovícico y el Jurásico, y totalmente ausentes en los mares de aragonita del Pérmico.
Los fósiles y organismos invertebrados que se encuentran en depósitos asociados a mares de calcita suelen presentar conchas primas y esqueletos de calcita.
En estos casos, algunos organismos pueden presentar una capa externa de calcita y una interna de aragonita; esto se da por la rápida disolución que presenta la aragonita en mares calcítics; al ser precipitada como biominerales y no estar en contacto con el agua se mantiene.
Los mares de calcita coinciden con épocas de rápida expansión del fondo marino y con condiciones climáticas tipo invernadero (greenhouse).
Los centros de expansión del fondo marino a través de chimeneas hidrotermales reducen el ratio entre magnesio y calcio en el agua del mar. La relación del ratio Mg / Ca favorece la precipitación de la calcita en detrimento de la aragonita.
Un aumento de la expansión del fondo marino implica un aumento de la actividad volcánica, así como de los niveles de dióxido de carbono de la atmósfera y los océanos. Esto influye directamente en la precipitación de los polimorfos de CaCO3.
La calcita en los seres vivos, los fósiles y los procesos de fosilización
Los procesos de fosilización son complejos y presentan diferentes y numerosos estadios, desde el entierro hasta el descubrimiento del fósil.
Los organismos con partes duras como conchas mineralizadas presentes en trilobites o ammonites (entre otros organismos), presentan más opciones de ser conservados que los organismos con sólo partes blandas como las medusas o los gusanos.
Normalmente las partes conservadas en fósiles son las duras, ya que las blandas, constituidas principalmente por materia orgánica se descomponen. Aunque las partes duras pueden ser destruidas por la acción de las olas o comidas por otros organismos como hongos o algas, es más fácil que se preserven.
La posibilidad de que un organismo fosilizado, aumenta si éste ya vive en el sedimento; y aquellos que viven en el fondo marino son más fácilmente fosilizados que los que viven en la columna de agua.
La calcita es un mineral que tiene una elevada presencia en algunos organismos fósiles:
En el caso de los equinodermos, su tejido esquelético se compone principalmente de calcita rica en magnesio ((Ca, Mg) CO3).
Un caso curioso es el de las espículas; aunque estas pueden hacer más de 10 centímetros de largo, se comportan como monocristales cuando se observan con luz polarizada.
Los equinodermos también suelen presentar los huesecillos formados por material calcáreo. Los huesecillos son elementos que forman parte del esqueleto de ciertos equinodermos y que aportan más rigidez y protección.
Se encuentran de diferentes maneras en erizos de mar, estrellas de mar, ophiuroidea, pepinos de mar y crinoideos.
Los huesecillos (así como las espículas, que son huesecillos especializados) son las partes de los equinodermos que presentan una fosilización más favorable.
Algunos artrópodos como los trilobites, presentaban los exoesqueletos mineralizados, probablemente a partir de una mezcla de calcita y materia orgánica (quitina), exceptuando el orden Nektaspida; actualmente lo que se conoce más detalladamente es la presencia de calcita en los ojos de los trilobites.
Los ojos de los trilobites se han conservado en el registro fósil para que las lentes oculares y las estructuras que las rodean eran de calcita, un material difícil de descomponer.
Los ojos de calcita de los primeros trilobites eran una serie de lentes hexagonales herméticamente compactos, similares a los ojos compuestos de algunos artrópodos actuales.
Durante aquella época había grandes cantidades de calcita en el mar, por lo tanto, no había problemas a la hora de formar los ojos. Actualmente se han descrito tres tipos de ojos en los trilobites, todos ellos formados por calcita:
- Ojos holocroals: presentes en la mayor parte de los trilobites conocidos. Presentan hasta 15.000 lentes de calcita, y la membrana de la córnea sólo cubre las que se encuentran juntas.
- Ojos esquizocroals: este tipo de ojos se consideran una innovación respecto a los anteriores, y está presente en los phacòfids. Presentan un menor número de lentes (alrededor de unas 700), pero estas son de tamaño mayor. Cada una de las lentes tiene una córnea individual y se encuentran separadas entre ellas. La córnea penetra en las lentes.
- Ojos abatocroals: sólo se han descrito en el género Eodiscina del Cámbrico. Presentan unas 70 lentes de tamaño pequeño y separadas entre ellas con córneas individuales. La córnea no penetra en las lentes.
Además de los trilobites, diferentes especies de crustáceos y miriápodos también utilizan la calcita para la génesis de sus exoesqueletos.
En estos casos, la calcita puede llegar a suponer más del 40% de la cutícula. En cuanto a los moluscos con concha, presentan generalmente carbonato en esta, aunque también pueden generar conchas de otros materiales.
Hay varios grupos de moluscos que presentan conchas carbonatadas, como los bivalvos, gasterópodos, los polyplacophora, los ammonites o los nautiloïdeus, entre otros.
Las conchas calcáreas son formadas generalmente por calcita y / o aragonita, aunque algunos estudios también describen la presencia de vaterita.
Los cristales de carbonato cálcico se forman entre capas de materia orgánica. Generalmente, la cáscara de los moluscos está constituida por varias capas, generalmente de calcita y aragonito y posee una microestructura especial característica de cada cáscara.
Sin embargo, las cáscaras puramente calcítiques son extremadamente raras y se presentan sólo en bivalvos del género Ostreoida (como por ejemplo Crassostrea gigas); sin embargo, estos organismos presentan el miostracum (zona de adherencia de los músculos) aragonític, como cualquier otro bivalvo.
En la formación de conchas de los moluscos, la cáscara se forma a partir de un fluido orgánico secretado por las células del organismo, este fluido posteriormente es calcificado.
Para la formación de conchas, los iones calcio y carbonato son esenciales para que la cáscara es principalmente carbonatada; se considera que los iones calcio son tomados del agua marina y de los alimentos, aunque todavía hay controversia al respecto.
Los poríferos, también conocidos como esponjas, son animales con un registro fósil presente desde el período ediacárico.
Dentro del filo se pueden diferenciar tres clases: Demospongiae, Hexactinellida y Calcarea. Las dos primeras presentan espículas silíceas, mientras que la última las presenta calizas.
En el caso de las esponjas de la clase Calcarea, presentan espículas biominerales de hasta 10 mm de longitud y con formas específicas; están formadas por calcita rica en magnesio.
Las espículas se encuentran cubiertas por una especie de vaina orgánica. Estas espículas se comportan como individuos monocristalinos de calcita y en cierto modo la orientación cristalográfica está relacionada con la morfología.
A pesar de su naturaleza monocristalina, la mayoría de espículas presentan un comportamiento de fractura casi isótropo, nada típico de los cristales de calcita, lo que indica una mayor resistencia de las espículas.
Cada espícula se encuentra formada por células especializadas que suministran iones minerales en cavidades extracelulares, donde se produce la cristalización a través de un cristal núcleo.
Podemos comparar las espículas calcítiques de las esponjas calcáreas con las silíceas del resto de esponjas y con los equinodermos.
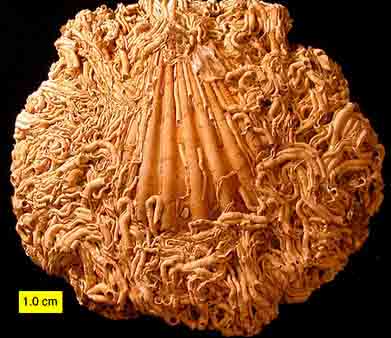
Además, los elementos esqueléticos de los equinodermos se asimilan a las espículas calcáreas de las esponjas, sobre todo por el hecho de ser, en ambos casos, elementos formados por cristales individuales de calcita magnesianas que forman estructuras complejas.
Dentro de los poríferos se encuentran dos especies fósiles relevantes: los estromatopòrids y los archaeocyatha.
Los estromatopòrids (Stromatoporida) fueron poríferos que vivieron entre el Ordovícico y el Devónico, formando arrecifes con corales tabulados y briozoos.
Los estromatopòrids se presentan como grandes pelotas de carbonato cálcico, que en sección presentan una estructura similar a la de las escleroesponges.
Los archaeocyatha (Archeociata) son un género extinto exclusivos del Cámbrico inferior; eran poríferos de pequeño tamaño que formaban arrecifes.
El material esquelético consistía en poliedros microgranulars entrelazados, constituidos de carbonato cálcico (presumiblemente calcita) con ejes aleatoriamente orientados y sin espículas.
Las algas calcáreas son un grupo de organismos sin validez taxonómica y, dentro de este grupo, se incluyen algas que precipitan carbonato cálcico (CaCO3). Este tipo de algas pueden llegar a formar bioconstrucciones carbonatadas de cierto tamaño.
Normalmente el término se emplea para describir algas bentónicas e incluye especies de los clorófitos (Chlorophyta), rodòfits (Rhodophyta), Phaeophyceae y cianobacterias.
Generalmente, las clorofita precipitan aragonita mientras que las rodòfites precipitan calcita rica en magnesio. Las cianobacterias tienen un papel importante en la precipitación de calcita en ambientes lacustres, especialmente en lagos oligotróficos.
Los serpúlids son una familia de anélidos sésiles constructores de tubos. Estos tubos son exclusivamente de material carbonatado como la calcita.
Los serpúlids son importantes calcificadoras, sobre todo en mares templados, donde llegan a formar pequeños arrecifes. Los serpúlids tienen uno de los sistemas de biomineralización más avanzados de entre los anélidos y pueden construir tubos de calcita, aragonita o mixtas.
Usos de la calcita
Las propiedades de la calcita hacen que sea un mineral ampliamente utilizado. Se utiliza como material de construcción, abrasivo, pigmento, en la industria farmacéutica y otros.
La industria de la construcción es la principal industria consumidora de calcita, sea en forma de roca caliza o mármol.
Estas rocas se emplean como rocas para construcción o como mortero; se han empleado desde hace miles de años. Los bloques de calcita son los principales materiales de construcción en muchas pirámides de Egipto y América Latina.

La industria actual utiliza la calcita para producir cemento; el cemento se utiliza para construir edificios, carreteras, puentes, paredes y otras estructuras.
En el contexto de la construcción, la calcita también se utiliza ornamentalmente, ya sea en forma de mármol, travertino o blanda caliza.
La calcita también es el componente principal de la tiza (el utensilio que se utiliza para dibujar sobre las pizarras).
La calcita también se utiliza para la neutralización de ácidos. Durante cientos de años. Las calizas y los mármoles se han fragmentado y esparcido por los campos como neutralizadores de los suelos.
También se calientan para producir una reacción más rápida en el suelo.
La calcita también se emplea como neutralizador en la industria química, en áreas donde los ríos o corrientes de agua se encuentran afectados por drenaje ácido de minas; distribuyéndose en estas corrientes, la calcita ayuda a neutralizar los ácidos.
El carbonato de calcio derivado de calizas o mármoles de alta pureza también se utiliza en la medicina; mezclado con azúcar y potenciadores del sabor, el carbonato forma pastillas masticables para neutralizar los ácidos del estómago
Varios productos químicos importantes se producen también a partir de la calcita; sobre todo diferentes productos de higiene doméstica como los detergentes.
También es empleada para la fabricación de fertilizantes, metales, vidrio, gomas y cauchos, así como pinturas. La variedad transparente conocida como espato de Islandia se utiliza en la industria óptica para la fabricación de polarizadores de microscopios y otros utensilios.
La calcita molida, llamada blanco de España, se utiliza como abrasivo suave. Además, es uno de los mejores minerales para coleccionar, ya que hay muchas formas interesantes y variadas, así como coloridos y bonitos especímenes.
Son relativamente fáciles de identificar por los coleccionistas debido a su doble refracción y su reacción con los ácidos.
La calcita en forma de polvo se utiliza para diferentes propósitos. Cuando se utiliza en forma de polvo, la calcita menudo presenta un marcado color blanco, y por tanto se utiliza como pigmento o como emblanquinador; incluso, algunas pinturas primitivas fueron pintadas a partir de polvo de calcita.
El polvo extraída a partir de calizas o mármoles, es ampliamente utilizada como suplemento en piensos de animales: las gallinas ponedoras y las vacas lecheras necesitan importantes aportaciones de calcio para mantener su producci
La calcita, al ser un mineral de baja dureza (3 en la escala de Mohs), puede ser utilizado como abrasivo de baja dureza, para limpiar superficies sin dañarlas.
El polvo de caliza también puede ser aplicada sobre las paredes y el techo de minas de carbón para reducir el polvo derivada del carbón en el aire (polvo que conlleva peligro de explosión); el polvo de calcita no es inflamable y por tanto reduce este riesgo.
La calcita también puede ser utilizada como almacén de dióxido de carbono. El dióxido de carbono es un gas que ayuda a atrapar y mantener el calor en la superficie terrestre.
Durante el proceso de formación de calcita, parte del dióxido de carbono se elimina de la atmósfera y se almacena durante largos períodos de tiempo; cuando la calcita se meteorizado o se utiliza para algunos usos como la basificación de aguas o la producción de cemento, este proceso de almacenamiento del CO2 se revierte, por tanto, la generación y destrucción de calcita tiene un importante papel sobre el clima terrestre.
Variedades
Existen muchas variedades de calcita. Algunas de estas variedades son conocidas por su forma cristalina, por sus propiedades, o bien por su composición química.
En cuanto a su forma, una de las variedades más conocida es la llamada calcita diente de perro, con cristales escalenoedres los que presentan la forma dipiramidal similar a los dientes de los caninos.
La calcita alas de ángel es una variedad determinada tanto por la forma de los cristales como por su color.
Los cristales son grandes, muy delgados y tabulares, de color blanco, asemejándose a las alas de los ángeles.
Generalmente son más gruesos en la base, e incoloros en el interior de las zonas más gruesas. Se trata de una variedad común de México
En cuanto a sus propiedades, la variedad más conocida es el llamado espato de Islandia, que son fragmentos de calcita totalmente incoloros y transparentes.
Fue encontrado por primera vez en cavidades basálticas de Islandia y muestra con mucha claridad el fenómeno de la birrefringencia o refracción doble, que hace que los objetos se vean a través de este aparezcan doblados.
A una longitud de onda de ~ 590 nm la calcita tiene un índice de refracción ordinario y extraordinario de 1,658 y 1,486, respectivamente.
Otro ejemplo de variedad bastante conocida es el ónix mexicano, una variedad de calcita usada con propósitos ornamentales que se corta con facilidad en pequeñas figuras, vasos y otros objetos comunes (no debe confundirse con el verdadero ónix, el cual es una variedad criptocristalina del cuarzo).
Hay una variedad denominada tradicionalmente alabastro que no debe confundirse con la variedad de yeso llamada también alabastro. Ambos tipos de alabastro han sido utilizados como piedra ornamental debido a su estructura de cristales especialmente hasta susceptible de ser pulida, con un bel blanco translúcido.
En esta variedad de este mineral (a menudo formada en ambientes sedimentarios detríticos) los cristales son muy pequeños (prácticamente invisibles a simple vista) formando un gran volumen masivo de roca caliza.
La glendonita es una variedad de calcita pseudomórfica tras ikaïta, originaria de Glendon (Nueva Gales del Sur, Australia).
La ikaïta es una especie mineral con fórmula química CaCO3 · 6H2O bastante inestable, ya que se deshidrata este mineral por encima de los 8 ° C. El gennoishi es una variedad de glendonita.
Otras variedades de calcita son: afrita, antraconita (una variedad carbonífera negro, a menudo bituminosa), argentina o espato Schieffer (una variedad laminar con brillo plateado), baricalcita (una variedad que contiene bario, con fórmula ((Ca, Ba) CO3)
Barleycorn (una variedad que consiste en pseudomorfismes, posiblemente de gaylussita), bruyerita (una variedad concreciones negro), capreïta, la que tiene cabeza de llave (una variedad con una terminación piramidal plana de los cristales prismáticos, asemejándose a una cabeza de llave), cobaltocalcita (una variedad de color rosado debido a su contenido de Co2 +)
La especie palomita (una variedad que cristalizó en pequeños nódulos; al romperse el material, las superficies resultantes se parecen a un montón de palomitas de maíz)
Otras especies son la dolomítica (una variedad que contiene pequeñas cantidades de magnesio en sustitución del calcio), calcita estròncica (que contiene estroncio), la variedad férrica (que contiene hierro), calcita magnésica (rica en magnesio), calcita mangànica o manganocalcita (rica en manganeso), calcita niquèlica (una variedad que contiene níquel)
Calcita plúmbico (que contiene plomo), calcita-arena (una variedad con los cristales crecidos con inclusiones de arena), calcita zíncica (variedad rica en zinc), crazy calcita (nombre que se aplica en el ámbito local en Nueva Jersey a una variedad masiva que emite fluorescencia en dos tonalidades e intensidades de rojo bajo onda corta ultravioleta)
Drewita, espato pizarra (una variedad lamelar), espato satinado (que no debe confundirse con el espato que es una variedad de yeso), hematoconita (de color rojo sangre coloreada debido a las inclusiones de hematites), hay slopita, lublinita (una forma eflorescente y suave, con consistencia fibrosa, y en generalmente húmeda)
Jade mexicano (de color verde teñida artificialmente), patagosita, pelagosita ( una delgada capa oscura sobre dolomita, posiblemente formada por la acción del agua de mar), prasocroma (rica en óxido de cromo, que se encuentra como un recubrimiento producto de alteración de la cromita), prunnerita (violeta similar a la calcedonia), pseudogaylussita (pseudomórfica tras gaylussita)
Roepperita, stinkkalk (una variedad que se distingue por desprender un olor fétido al fracturarse la debido inclusiones de H2S), y travertino (formado por carbonato de calcio disolvente en agua subterránea y luego depositándolo en la superficie de la tierra por los ríos, fuentes naturales, o géiseres)